Le plus grand défi auquel le laboratoire Moderna a été confronté lorsqu'il a décidé de rechercher et de produire une nouvelle génération de vaccins contre le COVID - les vaccins dits bivalents - était de savoir comment il allait surmonter le plus grand atout laissé par la pandémie : un stock important de vaccins de sécurité et l'efficacité des inoculants vaccinaux de première génération, produits en un temps record, avec des développements scientifiques innovants et prouvés pour sauver des millions de vies sur la planète.
Il faut dire aussi que la course dans le temps de toutes ces innovations pour le COVID, et de plus en plus étendue à d'autres maladies respiratoires, s'est montée sur l'autre clé d'or laissée par le temps de la pandémie : la plateforme génétique des ARN messagers .
D'un pas ferme et déterminé, le laboratoire Moderna -originaire des États-Unis- a profité de ce contexte de grande opportunité pour la science et est allé plus loin : la production à l'échelle mondiale du premier vaccin de rappel bivalent contre le COVID -pour adultes- dans ses deux versions , la 1273.214 - composée de 25 microgrammes contre le variant et/ou la séquence ancestrale de Wuhan, et l'autre restante de 25 mg contre le variant Ómicron BA1 ; et le second - 1273.222 - qui est actuellement appliqué aux États-Unis - fabriqué avec 25 microgrammes contre la variante Wuhan et les 25 autres mg contre les variantes Omicron BA4 et BA5.
En dialogue avec Infobae, via zoom, du Massachusetts, Rolando Pajón , directeur médical scientifique pour l'Amérique latine de Moderna et qui a dirigé depuis le début le projet scientifique des vaccins de rappel bivalents du laboratoire nord-américain, est parti d'une idée très éclairante sur la état actuel de la pandémie, et a expliqué : « Les vaccins bivalents ou de deuxième génération apparaissent comme un instrument clé et opportun dans cette période de transition de la pandémie. Elles représentent aussi le prélude à aller vers une annualisation du calendrier vaccinal contre le COVID. Et ils viennent confirmer que pour mettre fin à la pandémie il est indispensable d'atteindre la pérennité de la réponse immunitaire des vaccins. C'est la clé de tout."
Pajón, avant Infobae , a ajouté, depuis Cambridge, aux États-Unis, où se trouve le siège du laboratoire moderne : « Nous travaillons avec des vaccins pan-respiratoires, ce seront tous des vaccins à plateforme génomique (ARN messager), qui se combinent en un seul injection, des anticorps contre trois virus. Par exemple : un vaccin contre le COVID + un candidat vaccin contre le virus respiratoire syncytial + un troisième candidat vaccin avec la dernière mise à jour du virus Influenza. Ceci dans Moderna est déjà planifié et en cours d'exécution.
- Combien de temps estimez-vous qu'il manque pour l'apparition des vaccins pan-respiratoires ? - Infobae consulté.
— Rolando Pajón : Nous estimons les vaccins pan-respiratoires dans les 3 à 5 prochaines années . Le plus proche, avant fin 2022, est d'avoir la combinaison entre le bivalent COVID (variant ancestral de Wuhan + variant BA4-BA5) et le vaccin contre la grippe.
bonnes nouvelles
Changer le paradigme des vaccins COVID n'allait pas être quelque chose d'anodin, cela allait demander de la dynamique et de la flexibilité de la part des esprits brillants des firmes pharmaceutiques, et surtout d'avoir une vision à long terme. Moderna a pu répondre à ces exigences. Il était décisif de très bien faire la preuve de concept avec les bivalents, où l'efficacité, la sécurité et la tolérance ont été démontrées, mais ce n'était pas un produit.

Moderna testé avec un "premier bivalent" -qui n'était pas un produit- où il se combinait dans les 50 microgrammes disponibles dans le vaccin COVID, 25 mg contre la variante/séquence ancestrale de Wuhan et 25 mg supplémentaires contre la variante Beta, qui était celle qui a déclenché "la" question initiale qui a donné lieu à l'essai clinique des bivalents.
Pajón, docteur en biochimie et biologie moléculaire et diplômé de l'Université de La Havane, Cuba, son pays natal bien-aimé, a souligné: «La question initiale de notre essai clinique s'est posée il y a plus d'un an lorsqu'il est arrivé, ce que nous avons initialement appelé le Variante sud-africaine, que nous appellerons plus tard Beta. La variante bêta a été la première à présenter un groupe de mutations, dans sa protéine de pointe, qui sont là dans le but d'échapper à la réponse immunitaire offerte par les vaccins. La variante Alpha avait d'autres types de mutations, y compris la Delta qui est venue plus tard, mais elles n'étaient pas aussi efficaces pour échapper à la réponse immunitaire. Beta a été le premier à le démontrer. Là on s'est rendu compte qu'on allait devoir mettre à jour les vaccins, si ce processus d'évolution des variants vers la fuite et l'évasion se poursuivait ».
Aujourd'hui, Moderna propose deux boosters bivalents contre le COVID -approuvés par la FDA (Food and Drugs Administration) et l'EMA (European Medicines Agency) - qui contiennent de l'Omicron - le premier, Wuhan + Omicron BA.1 et le second, Wuhan + Omicron BA.4 et BA.5 - qui ont tous deux démontré une plus grande réponse immunitaire que la première génération chez les adultes .
Ils ont également testé la pérennité de la réponse immunitaire, qui sera la clé du passage de la pandémie à l'endémique (fin de la pandémie), et la confirmation de l'annualisation du calendrier vaccinal contre le COVID , au lieu de devoir être en retard les renforts tous les six mois.
— Comment les autorisations réglementaires pour les bivalents ont-elles été obtenues, d'abord FDA puis EMA ou inversement ?
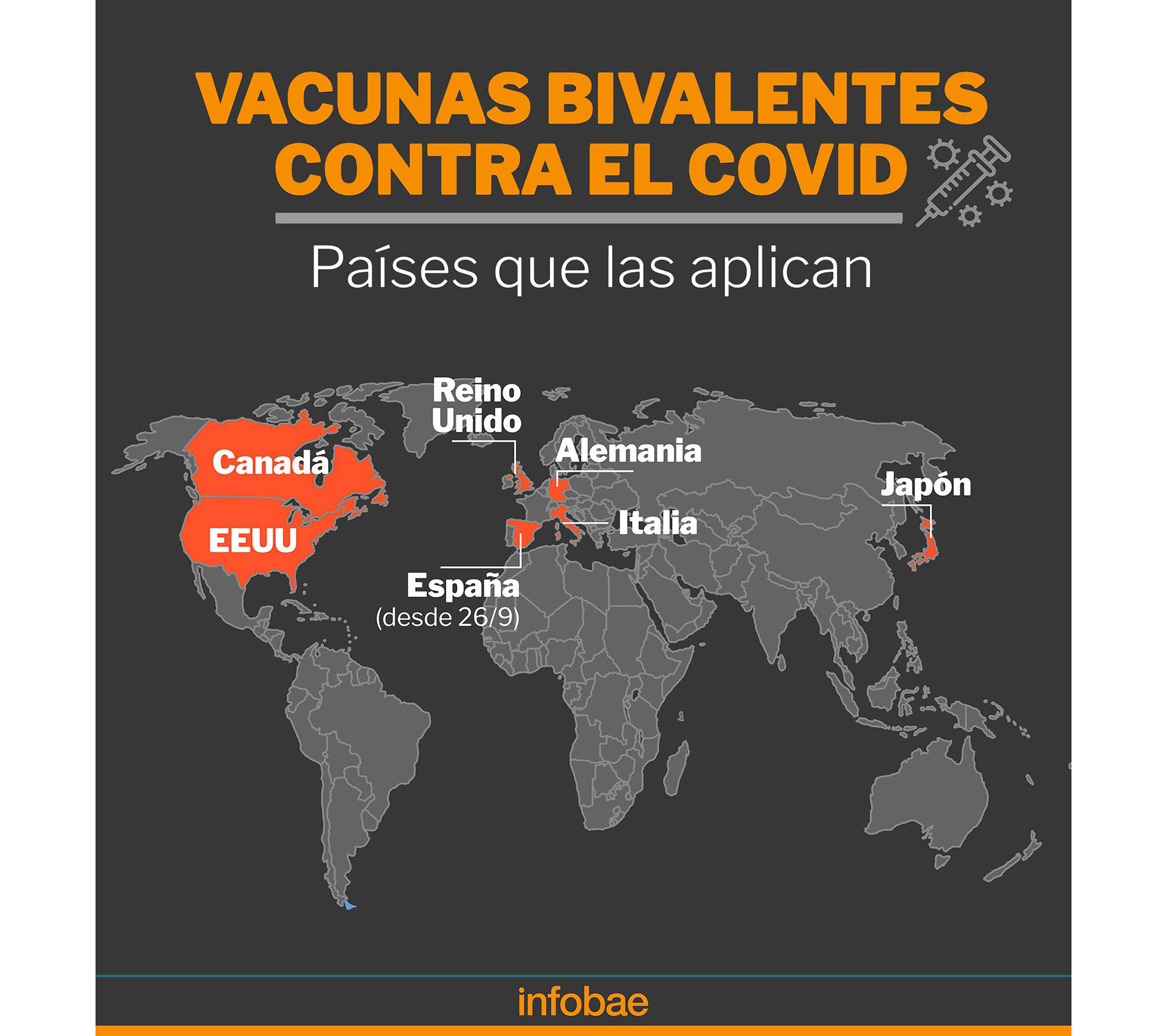
— Rolando Pajón : Dans ce cas, les pays individuels sont venus en premier. Le premier pays à autoriser les bivalents fut l'Angleterre. Maintenant, la carte s'est agrandie. Nous travaillons en collaboration avec les agences de réglementation -FDA et EMA- ; et ils ont publié des directives pour identifier les données dont ils avaient besoin pour dire qu'un vaccin mis à jour est quelque chose qu'ils allaient approuver. Les récentes approbations bivalentes ont démontré que les organismes de réglementation vont commencer par les plateformes qu'ils comprennent le mieux.
Moderna a reçu des décisions d'autorisation pour l'utilisation de nos bivalents de renforcement contenant de l'Omicron dans les pays et régions suivants : États-Unis, Australie, Canada, Europe, Japon, Corée du Sud, Suisse, Taïwan et Royaume-Uni.
Dans tout vaccin adapté, nous ne pouvons pas perdre ce que nous avons. Nous devons améliorer ce que nous avons ! Et de là émerge le concept bivalent. Le bivalent a deux composants. Un des composants est à 50% du vaccin à séquence originale -Wuhan- présent à 100% dans les vaccins originaux ou de première génération. Et les 50% restants sont la séquence ou variante circulante dominante qui présente la capacité d'échapper à l'immunité vaccinale - pour l'instant, Omicron -.

— Quelles ont été les étapes scientifiques clés que Moderna a franchies pour lancer l'approbation et le développement de ce nouveau segment de vaccins bivalents ou de deuxième génération ?
—Rolando Pajón : En plus d'être fiers du chemin scientifique que nous avons exploré avec rapidité et cohérence depuis Moderna, la première chose que nous avons comprise est l'évasion, l'évasion que le virus du SRAS-CoV-2 avait avec les vaccins de première génération . Nous travaillons avec les agences réglementaires pour définir les lignes de travail et créer de nouveaux vaccins mis à jour, les bivalents. La séquence/variante de Wuhan qui est à la base du vaccin que nous avons largement utilisé dans le monde et qui a sauvé de très nombreuses vies représentait 50 % du nouveau vaccin ; et l'autre moitié du contenu proviendrait d'une variante qui circule . Nous avons été les pionniers dans la création de ce concept bivalent.
Lorsque nous testions la variante Wuhan + Beta dans la preuve de concept, nous avons constaté que la sécurité et la tolérabilité ne changeaient pas. En d'autres termes, le profil que nous connaissions des effets indésirables était le même. C'était très important.

Je veux dire, si au lieu d'utiliser les 50 microgrammes de la séquence de Wuhan, nous utilisons maintenant 25 mg de Wuhan, plus 25 mg d'une nouvelle séquence, que se passe-t-il ? la réponse du point de vue de la sécurité et de la tolérance est : rien, c'est exactement la même chose. Nous avons également vu que la réponse immunitaire avec les bivalents était supérieure et plus durable.
La clé de cette transition pandémique est de disposer d'un vaccin capable d'influencer une réponse immunitaire de longue durée. Nous pensons que la plateforme bivalente est vraiment la réponse, à tel point que nous travaillons également sur le développement combiné de notre vaccin COVID avec notre candidat vaccin Influenza et notre candidat vaccin respiratoire syncytial . La grippe et le syncytial respiratoire sont déjà en phase 3 .
Le COVID bivalent est notre meilleure option pour y parvenir : nous voulons l'étendre à un multivalent, pan-respiratoire, où avec une seule ponction par an, vous êtes protégé contre la variante COVID bivalente qui circule, la nouvelle grippe et le virus respiratoire syncytial. .
—Pensez-vous que les vaccins bivalents sont le véritable instrument scientifique et thérapeutique contre le COVID pour pouvoir décréter la fin de la pandémie ?
—Rolando Pajón : Clairement oui ! Aujourd'hui, Moderna propose deux bivalents qui, avec une seule injection, ont démontré une plus grande réponse immunitaire. Ce que j'ai moi-même appelé la pérennité de la réponse immunitaire qui sera la clé de la pandémie jusqu'à la fin de la pandémie. C'est aussi la porte ouverte sur ce qui est à venir : les vaccins à plateforme génomique pan-respiratoire (ARN messager). Associez dans une même injection un vaccin contre le COVID + un autre contre le virus respiratoire syncytial et un vaccin Grippe actualisé. Ceci dans Moderna est déjà planifié et en cours d'exécution

Dans les 10 prochaines années, la mission scientifique loin d'être simple que nous nous sommes fixée à Moderna est d'éliminer les maladies respiratoires grâce à des vaccins à base d'ARN messager.
Nous voulons éliminer les hospitalisations et les décès dus à des maladies causées par des virus respiratoires. En d'autres termes, nous voulons disposer dans 10 ans d'un vaccin pan-respiratoire suffisamment efficace pour garantir que nos populations âgées ne souffrent pas de ces maladies , ces syndromes respiratoires viraux récurrents que nous avons à chaque saison.
— Quelle est la place des pédiatres dans toute cette chaîne d'innovations ? Il semble que la vitesse que Moderna donne au développement de vaccins contre le COVID et autres chez l'adulte, ne s'applique pas à la pédiatrie
« La rapidité avec laquelle nous sommes et avons été dans le développement de vaccins à ARN messager pour adultes est proportionnelle à notre prudence dans le secteur pédiatrique. Notre prochaine étape est sans aucun doute d'amener les bivalents en pédiatrie. Avant la fin de l'année, nous évaluerons les doses de rappel de notre bivalent dans l'espace pédiatrique.

Nous avons une conscience et une éthique de travail qui nous amène justement à valider tout ce que nous faisons dans une tranche d'âge avant de passer aux âges pédiatriques. Nos bivalents sont actuellement en cours d'examen et d'autorisation par différents pays pour une utilisation chez l'adulte . Que se passe-t-il ensuite ?
Une étude clinique ne s'arrête pas lorsque nous avons déjà généré les données que nous voulions . Ces études doivent être poursuivies et elles sont importantes car des données supplémentaires sur la réponse immunitaire, l'efficacité, la sécurité et la tolérance dans le temps y sont générées.
Différents pays et organismes de santé commencent à mener des études dans le monde réel du bivalent. Nous devons analyser toutes ces informations qui sont générées, et les organismes de réglementation doivent également analyser ces données.
— Avec un système scientifique mondial qui pendant la pandémie a démontré sa capacité à travailler ensemble, sa rapidité et son efficacité, comment résoudre les problèmes de santé dans le monde, la question de l'accès et des inégalités entre les pays ? Il existe encore de nombreuses poches de personnes non vaccinées dans des pays très pauvres... Que se demande une entreprise comme Moderna et que pense-t-elle de ces questions ?
— Lorsque la FDA nous a autorisé - en décembre 2020 - notre vaccin COVID en utilisation d'urgence, déjà à ce moment-là nous avions la preuve biologique, scientifique et médicale que tout fonctionnait bien...

Cependant, ce fut une journée de sentiments mitigés. Parce qu'on s'est rendu compte qu'on avait un vaccin qui pouvait sauver le monde, mais on n'allait pas pouvoir sauver tout le monde en même temps. Parce que nous n'allions pas pouvoir produire toutes les doses dont nous avions besoin. Cela allait prendre du temps. Et cette attente pour augmenter notre capacité de production était vraiment très pénible .
Que pouvons nous faire? Comment pouvons-nous nous assurer que nos vaccins à ARN, présents et futurs, atteignent tous les coins ? il faut d'abord générer une capacité de production suffisante. Et nous y sommes parvenus. Nous avons réussi à générer une capacité de production très élevée qui couvre les besoins du monde. D'autre part, continuez le travail inlassable avec les gouvernements et les organisations. Nous parlons à tout le monde et recherchons différents types de solutions pour essayer de conclure des accords. Notre objectif est de faire parvenir ce vaccin aux gens.
vision et rupture
La vision de Moderna de l'avenir de l'industrie pharmaceutique, en plus d'être révolutionnaire, peut même être utopique pour certains. Le Dr Pajón a déclaré à Infobae : « Il y a des maladies qui ne font pas partie des priorités des entreprises du premier monde. De Moderna nous proposons une plateforme ouverte, et démocratisant l'accès, rapide et efficace. Notre plateforme d'ARN messager nous permet, avec une seule usine, de fabriquer des vaccins contre de nombreux pathogènes. Le processus de production est exactement le même . C'est un grand avantage . Actuellement, dans le cadre de la stratégie globale, nous avons des centres de production d'ARN messager à l'extérieur de l'Amérique du Nord. Nous avons établi un centre de production et des accords au Canada, en Australie, au Kenya, en Afrique et en Suisse ».

Pajón a décrit ce processus avec un exemple simple et compréhensible : « Chez Moderna, nous serions comme un téléphone Iphone - une plate-forme qui fonctionne d'une certaine manière ; et les différents partenaires ou associations que nous établirons dans le monde seront les applications iPhone. Et ils vous permettent d'utiliser le téléphone à votre guise. Chaque pays sera en mesure de concevoir, de prioriser et d'établir des priorités pour les vaccins et autres thérapeutiques. Nous leur donnons l'iPhone ». Une approche plug-and-play.
Pour promouvoir le -pour l'instant- appelé Moderna's RNA Project (DART, pour son acronyme en anglais pour Deployable Accelerated RNA Technology), nous travaillons avec des agences internationales sur ce que nous appelons les quinze maladies prioritaires. Et l'engagement de l'entreprise nord-américaine - dont le PDG est l'innovateur, Stéphane Bancel - est dans les cinq prochaines années d'avancer avec des candidats vaccins dans ces quinze maladies.
CONTINUER À LIRE
