
C'est que cette vaccination a déjà été évaluée chez 100 volontaires , âgés de 18 à 60 ans, et dans les semaines à venir, les inscriptions s'ouvriront pour avancer avec une deuxième étape dans 10 centres à travers le pays. “Es el resultado de la enorme tarea realizada por nuestras científicas y científicos y del trabajo conjunto entre el Ministerio de Ciencia, el Ministerio de Salud, el CONICET , la UNSAM y el Laboratorio Cassará ”, señaló Filmus durante su presencia en la Universidad Nacional de San Martin.
"Ce vaccin est une source de fierté pour l'Argentine et représente un exemple vertueux d'articulation public-privé", a ajouté le ministre, qui était accompagné du président de l'Agence R+D+i, Fernando Peirano. A noter que cette phase a bénéficié d'un financement de 1 100 millions de pesos par l'Agence R+D+i, dépendante du MINCyT.
Cette vaccination, suivant les recommandations des spécialistes et des agences de santé locales et internationales, permettra également de débuter l'évaluation d'une nouvelle version bivalente de la formule, avec un antigène Omicron BA.4 et BA.5 . Et selon les avances à Infobae du laboratoire Pablo Cassará, ils ont déjà la capacité industrielle de produire jusqu'à 5 millions de doses mensuelles d'antigène vaccinal, et ils prévoient de démarrer leur fabrication parallèlement au développement des études de phase II/III susmentionnées. .

« Nous sommes vraiment très heureux de pouvoir commencer cet essai. L'ARVAC Cecilia Grierson est le premier vaccin argentin à atteindre les phases 2 et 3 d'évaluation. Dans cette étape, 100 volontaires âgés de 18 à 60 ans ont déjà été vaccinés et, bientôt, l'inscription s'ouvrira pour avancer avec une deuxième étape dans 10 centres à travers le pays qui comprend des essais sur 1 800 personnes de plus de 18 ans, dans certains cas, avec des comorbidités », a expliqué Cassataro, biologiste (UNSAM), docteur en immunologie et chef de l'équipe UNSAM-CONICET qui travaille sur ce vaccin. Alors que l'étude de phase II/III a l'incorporation et la contribution du groupe de travail du médecin et chercheur Gonzalo Pérez Marc.
Chronologie d'une percée argentine
Après avoir obtenu des résultats positifs en phase I, dans les premiers jours de 2023, l'Administration nationale du médicament, de l'alimentation et de la technologie médicale (ANMAT) a autorisé le démarrage des études de phase II/III. À ce stade, les experts cherchent à évaluer l'innocuité, la tolérabilité et l'immunogénicité de l'inoculant ; étant donné qu'ARVAC est un vaccin protéique produit par biotechnologie, une plateforme technologique très sûre qui est utilisée depuis des décennies dans les inoculations pour les nouveau-nés et les adolescents. En fait, Cassará a développé et lancé le premier vaccin contre l'hépatite B produit dans la région en 1997.
« Ce type de technologie (produit à base de protéines recombinantes) se conserve au réfrigérateur (2 – 8 °C) et peut durer un an ; par conséquent, pour la distribution dans des endroits éloignés où ils n'ont pas accès à un congélateur à -70, c'est important. Et un autre problème est que cette plate-forme a déjà une capacité de fabrication dans la région. Il existe déjà des usines qui produisent des anticorps monoclonaux et elles peuvent les fabriquer dans tout le pays », avait souligné un autre des scientifiques en charge du développement, Juan Manuel Rodríguez , biologiste (UBA) et coordinateur du domaine R&D. Infobae.D de biopharmaceutique du Laboratoire et Fondation Pablo Cassará.
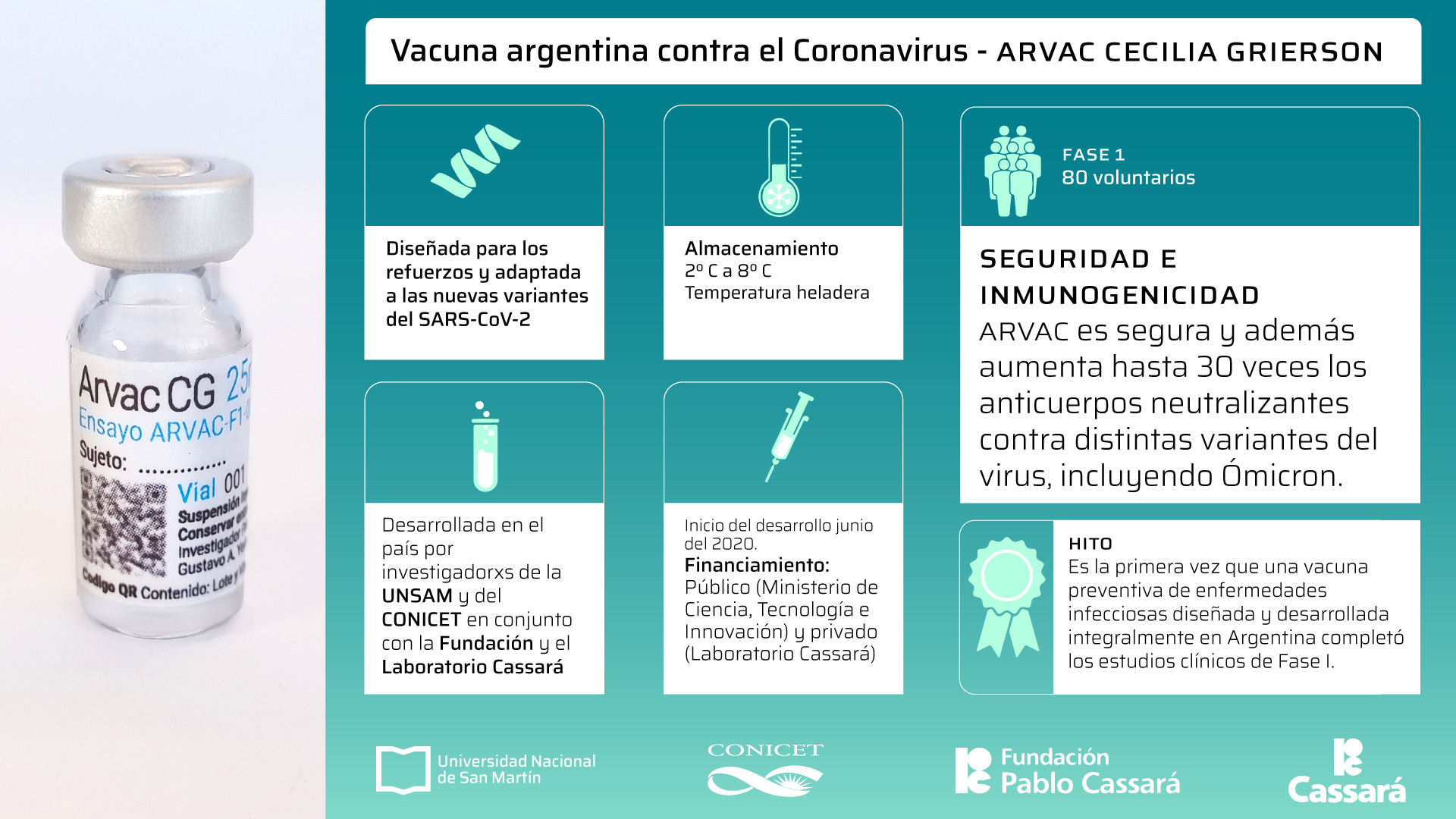
Au cours du processus technologique à l'échelle industrielle de l'ARVAC, qui a débuté en 2021, 5 technologies de production d'antigènes ont été développées dans les variantes SARS-CoV-2 Wuhan, Gamma, Delta, Omicron B1 et Omicron BA.4 et BA. Dans l'étude de phase I, il a été constaté que la formule est sûre et qu'elle augmente jusqu'à 30 fois les anticorps neutralisants contre Wuhan, Gamma et Ómicron. ARVAC est conçu comme un vaccin de rappel, il peut être conservé et transporté réfrigéré entre 2°C et 8°C et, de plus, son principe actif peut être mis à jour pour faire face aux nouvelles sous-lignées du virus qui échappent à la réponse immunitaire.
Une réalisation essentielle de la science argentine
La voie de ce vaccin a fait ses premiers pas avec un financement initial de l'Agence Nationale de Promotion de la Recherche, du Développement Technologique et de l'Innovation (Agence R+D+i) du Ministère de la Science et de la Technologie de la Nation. Le suivant était l'investissement du Laboratoire Cassará dans le développement technologique et dans les études de phase I. 4. C'est la première fois qu'un vaccin contre les maladies infectieuses conçu et développé entièrement en Argentine parvient à terminer les études cliniques de phase I.

« Il s'agit d'un projet qui concentre la capacité scientifique et technologique de l'Argentine sur la résolution de besoins spécifiques à fort impact sanitaire et économique. Le projet installera une plate-forme pour le développement et la production de vaccins recombinants qui pourront être utilisés pour de nouveaux vaccins à l'avenir », a déclaré à ce média Jorge Cassará, directeur du laboratoire homonyme.
Rappelons que, dans cette deuxième étape de Phase II/III, le vaccin sera inoculé à quelque 1800 volontaires pour que, courant 2023, l'ANMAT approuve son inoculation. Comme ils l'avaient détaillé auprès du ministère national de la Santé, dirigé par Carla Vizzotti, les études seront menées "chez des volontaires adultes préalablement vaccinés contre le virus SARS-CoV-2".
Continuer à lire:
